Laboratuvarımızın Kapalı Kapıları Ardında Embriyolarınızı Nasıl Değerlendiriyoruz?
Yardımcı üreme teknikleri, yani tüp bebek (ART) dünyasında, başarıyı belirleyen en temel faktörlerden biri kuşkusuz “embriyo kalitesi”dir. Ancak biliyorum ki bu kavram, sizler için bazen kafa karıştırıcı olabiliyor. Hatta biz embriyologlar arasında bile sürekli tartışılan, biyolojik karmaşıklığı çok yüksek ve teknoloji geliştikçe her gün yeni şeyler öğrendiğimiz dinamik bir konu bu.
Bu yazımizda, 2025 yılında güncellenen ESHRE/ALPHA İstanbul Mutabakatı (The Istanbul Consensus Update 2025) [1] ve yayınlanan literatür ışığında embriyo kalitesinin gerçekten ne anlama geldiğini, ölçümlerimizin bilimsel temellerini ve bu kararların tedavi sonucunuzu nasıl etkilediğini, hiçbir detayı atlamadan, şeffaf ve kapsamlı bir analizle sizinle paylaşacağız.
Embriyo Değerlendirmesine Tarihsel Bir Bakış
Tüp bebek tarihinin ilk yıllarında, embriyologlar embriyoları “güzel”, “çok güzel” veya “mükemmel” gibi oldukça sübjektif sıfatlarla tanımlarlardı. O zamanlar yaklaşımımız basitti: “Embriyo göze ne kadar hoş ve pürüzsüz görünüyorsa, tutunma ihtimali o kadar yüksektir.” Ancak zamanla bilimsel veriler biriktikçe gördük ki, bu sübjektif tanımlar laboratuvarlar arasında ortak bir dil oluşturmayı imkânsız kılıyor ve klinik sonuçları öngörmede yetersiz kalıyordu [1].
2011 yılında yayınlanan ilk İstanbul Mutabakatı, dünya genelinde ortak bir dil oluşturmayı hedeflemişti. Ancak aradan geçen sürede laboratuvarlarımızda büyük teknolojik değişiklikler yaşandı. Özellikle Sürekli Embriyo İzleme Sistemlerinin (Time-Lapse Technology – TLT) hayatımıza girmesiyle, embriyo gelişimi statik bir “fotoğraf karesi” olmaktan çıkarıp dinamik bir “film şeridi”ne dönüştürüldü. İşte 2025 yılında güncellenen yeni mutabakat, tam da bu teknolojik sıçramayı temel alıyor. Artık embriyo kalitesini sadece “görünüm” (morfoloji) ile değil, aynı zamanda “zamanlama” (kinetik) üzerinden tanımlayan yepyeni bir çerçeveyle çalışıyoruz.
Statik Gözlem mi, Dinamik İzleme (Morfokinetik) mi?
Geleneksel “statik” yöntemimizde, embriyolarınızı günde bir inkübatörden, yani o güvenli ortamından çıkarıp mikroskop altında inceleriz. Ancak bu işlem sırasında embriyo, çok kısa süreliğine de olsa ideal kültür ortamından uzaklaşmak zorunda kalır. Bu yöntemde iki temel kısıtlılığımız vardı:
- Gözlem Kısıtlılığı: Embriyo gelişimi yerinde durmayan, çok dinamik bir süreçtir. Örneğin, sabah 08:00’de baktığımızda 4 hücreli gördüğümüz bir embriyo, gece boyunca anormal bir bölünme yaşamış (örneğin 1 hücreden direkt 3 hücreye geçmiş) ve sonra kendini düzeltmiş olabilir. Statik gözlemle bu “ara olayları” ne yazık ki kaçırabiliyorduk [2].
- Çevresel Stres: Embriyonun dışarı çıkarılması, pH ve ısı değişimlerine maruz kalması demekti ki bu da gelişimsel stresi artırabiliyordu [4].
Buna karşılık, Time-Lapse teknolojisi sayesinde, inkübatör içine yerleştirilmiş kameralarla embriyolarınız dışarı hiç çıkarmadan, her 10-20 dakikada bir fotoğraflanıyor. Böylece sadece embriyonun son halini değil, o hale gelene kadar geçirdiği tüm serüveni (buna morfokinetik diyoruz) izleyebiliyoruz.
Terminoloji Karmaşasına Son: Derecelendirme, Sıralama ve Seçim
Raporlarınızda veya görüşmelerimizde sıkça duyacağınız üç terim arasındaki farkı netleştirmemiz, süreci anlamanız için önemli:
- Derecelendirme (Grading): Bu, embriyonun o anki objektif durumunun tarifidir. Hücre sayısı, simetrisi, fragmantasyon oranı gibi özelliklerine bakarak ona bir puan veririz (Örneğin; Grade 1, 4AA, 3BB gibi).
- Sıralama: Elimizdeki embriyoları, transfer önceliğine göre bir sıraya dizmemizdir. Örneğin 5 tane blastokistimiz varsa, bunları kinetik verilerine ve puanlarına göre “en yüksek gebelik potansiyeline sahip olandan en düşüğe” doğru sıralarız. Bu, “Hangisini önce transfer edeceğiz?” sorusunun cevabıdır.
- Seçim (Selection): Bu ise sıralama listesinden, sizin klinik özelliklerinize (yaşınız, geçmiş denemeleriniz, rahim durumunuz) ve varsa genetik test (PGT-A) sonuçlarınıza göre transfer edilecek nihai embriyonun belirlenmesidir. Yani seçim, sadece laboratuvar verisi değil, klinik bir stratejidir.
“Düşük dereceli” (low grade) bir embriyo, “kötü” demek değildir. Sadece sıralamada alt basamaklardadır ama biyolojik olarak canlı doğum potansiyeli taşıyabilir.
1. Gün: Zigot Dönemi
Spermin yumurtaya girmesiyle başlayan süreç, yaklaşık 16-18 saat sonra “Zigot” oluşumuyla görünür hale gelir. Bizim için ideal kontrol zamanı, işlemden sonraki 16-17. saatlerdir. Time-lapse sistemlerinde ise bu süreci dakika dakika izleriz; çekirdeklerin ne zaman belirdiğini (tPNa) ve ne zaman silindiğini (tPNf) kaydederiz.
Çekirdek (Pronükleus – PN) Sayısı
Normal bir zigotta biri anneden, biri babadan gelen iki çekirdek (2PN) görmeliyiz.
- 0PN (Çekirdek Görünmeyenler): Eskiden bunları “döllenmemiş” sayılır ve atılırdı ama Time-lapse verileri bize gösterdi ki, bazen çekirdekler çok hızlı oluşup kaybolabiliyor ve sabah kontrolüne gelindiğinde o evre kaçırılmış olabiliyordu. Eğer bu zigot bölünmeye devam ederse, sağlıklı bir blastokist olabilir.
- 1PN (Tek Çekirdek): Genellikle sadece annenin veya babanın genetiğini taşıdığı için (anormal) riskli kabul edilir. Ancak özellikle tüp bebek (IVF) vakalarında bazen iki çekirdek erken birleşmiş olabiliyor. Güncel veriler, 1PN’den gelişen blastokistlerin genetik testle (PGT-A) incelendiğinde bir kısmının normal çıkabildiğini gösteriyor.
- 3PN (Üç Çekirdek): Bu, genetik olarak anormal (triploid) bir durumdur ve kesinlikle transfer edilmez.
2. ve 3. Günler: Bölünme Aşaması
Zigot artık bölünüyor ve “embriyo” adını alıyor. Bu evrede en temel kalite kriterimiz hücre sayısıdır.
Hücre Sayısı: Altın Standart
Bölünme aşamasında zamanlamanın embriyo kalitesi üzerinde belirleyici bir faktör olduğu kabul edilmektedir. Döllenme işleminden yaklaşık 44 saat sonra (2. gün) gerçekleştirilen değerlendirmede, ideal bir embriyonun 4 hücreli yapıya ulaşmış olması beklenmektedir. Süreç 68. saate, yani 3. güne ulaştığında ise 7 ila 8 hücreli bir embriyo gelişiminin gözlenmesi hedeflenmektedir. Belirlenen bu referans aralıklarının dışına çıkılmasının, yani gelişimin 6 hücrenin altında kalarak yavaşlamasının veya 9 hücreyi geçerek aşırı hızlanmasının, embriyoda genetik hata (anöploidi) riskini artırdığı çeşitli çalışmalarda bildirilmektedir.
Fragmantasyon: Embriyonun “Kırıntıları”
Hücre bölünmesi esnasında sitoplazmadan kopan ve çekirdek içermeyen parçacıklar “fragman” olarak tanımlanmaktadır. Bu kapsamda yapılan derecelendirmede; %10’un altında fragmantasyon izlenen embriyolar Grade 1 (En İyi), %10-25 aralığındakiler Grade 2 (İyi), %25’in üzerindeki orana sahip olanlar ise Grade 3 ve 4 olarak sınıflandırılmaktadır. Klinik veriler ışığında, %25’in üzerindeki fragmantasyon oranının implantasyon başarısını olumsuz etkilediği görülse de, bu embriyoların bir kısmının sağlıklı blastokistlere dönüşebildiği saptanmıştır. Dolayısıyla, yüksek fragmantasyon varlığı tek başına bir imha sebebi olarak değerlendirilmemektedir.
Simetri ve Çok Çekirdeklilik (Multinükleasyon)
Hücrelerin eşit büyüklükte olması (simetri) istediğimiz bir durumdur. Ayrıca bir hücrenin içinde birden fazla çekirdek görülmesi (Multinükleasyon), özellikle 2. günde görülüyorsa risklidir. Ancak bu durumun geçici olabileceğini ve blastokist aşamasında düzelebileceğini de biliyoruz.
4. Gün: Morula Dönemi
Laboratuvar pratiğinde 4. gün genellikle “sessiz gün” olarak nitelendirilse de biyolojik düzeyde “Kompaksiyon” (Sıkışma) adı verilen kritik bir dönüşümün gerçekleştiği bilinmektedir. Bu evrede hücrelerin birbirine sıkıca kenetlenerek tek bir hücresel kitle halini aldığı gözlemlenmektedir. Değerlendirme sürecinde, tüm hücrelerin sıkışma sürecine dahil olduğu “Tam Kompaksiyon” izlenen morulalar en yüksek kalite sınıfında yer almaktadır. Bazı hücrelerin yapı dışında kaldığı “Kısmi (Parsiyel) Kompaksiyon” durumunun ise, embriyonun hasarlı hücreleri bünyesinden uzaklaştırarak kendini onarma (self-correction) mekanizmasını devreye soktuğu değerlendirilmekte olup, bu embriyoların da blastokist gelişim potansiyeli taşıdığı kabul edilmektedir.
5. Gün: Blastokist Aşaması
Döllenme sonrası sürecin en kritik evresi olan 5. günde, embriyonun yaklaşık 100-200 hücreli yapıya ulaşması beklenmektedir. Klinik raporlarda sıklıkla karşılaşılan kodların (örn. 5AA, 3BC) dayandığı Gardner Derecelendirme Sistemi, embriyo kalitesinin belirlenmesinde üç temel bileşen üzerinden değerlendirme yapmaktadır.
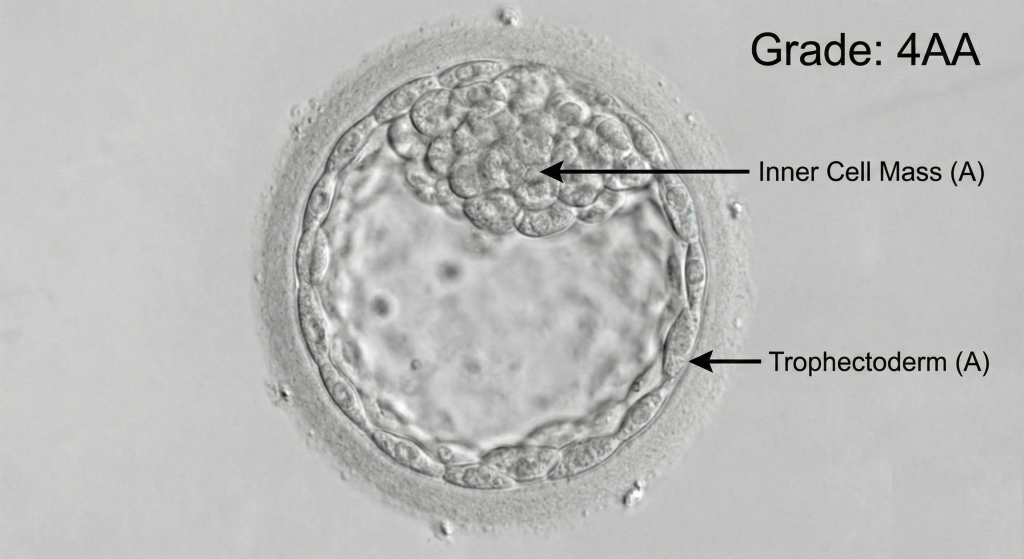
İlk olarak Genişleme Derecesi (1-6), blastokistin hacimsel büyüklüğünü ifade eder; burada “3” Tam Blastokist’i, “4” ideal transfer aşaması kabul edilen Genişlemiş (Expanded) yapıyı, “5 ve 6” ise implantasyona (tutunmaya) en yakın evreler olan Tomurcuklanan ve Zona’dan Ayrılmış (Hatching/Hatched) aşamaları temsil etmektedir. İkinci bileşen, fetüsü oluşturacak olan İç Hücre Kütlesi (ICM) olup ilk harf (A-C) ile kodlanmaktadır; çok sayıda ve sıkı paketlenmiş hücreler “A”, daha az ve gevşek yapılı hücreler “B”, sayıca yetersiz hücreler ise “C” (düşük ancak mevcut canlı doğum potansiyeli) olarak sınıflandırılmaktadır. Üçüncü bileşen ise plasentayı oluşturarak rahim içine tutunmayı sağlayan Trofektoderm (TE) tabakasıdır (İkinci Harf A-C); güncel çalışmalar, implantasyonun gerçekleşebilmesi için bu tabakanın hayati önem taşıdığını ve TE kalitesinin klinik başarıda belirleyici olduğunu göstermektedir.
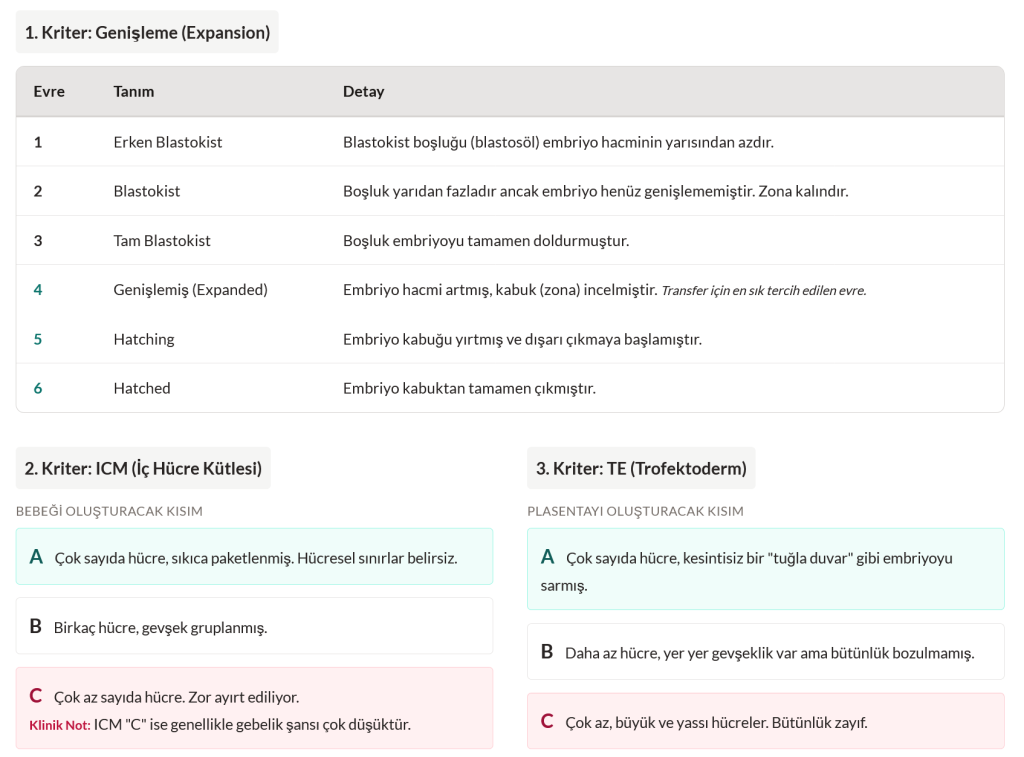
Örneklemek gerekirse; 5AA kodu, dışarı tomurcuklanan, mükemmel fetal ve plasental hücresel yapıya sahip üst düzey bir embriyoyu; 4BB kodu, genişlemiş ve iyi kalite hücresel özellikler gösteren (sıklıkla gebelikle sonuçlandığı gözlemlenen) bir embriyoyu; 3CC kodu ise hücresel yapısı zayıf, gebelik potansiyeli daha düşük (%15-20) olmakla birlikte genetik bütünlüğü korunduğu takdirde başarı şansı bulunan bir embriyoyu tanımlamaktadır.
“Embriyo kalitesi”nin, tek bir harf (A, B, C) veya rakamsal veri ile özetlenemeyecek kadar çok boyutlu bir kavram olduğu kabul edilmektedir. Bu çerçevede; en üst kalite (örn. 5AA) sınıflandırmasına sahip embriyoların dahi mutlak (%100) gebelik garantisi sunmadığı, başarının çok faktörlü bir süreç olduğu bilinmelidir. Öte yandan, düşük morfolojik kalite veya yavaş gelişim (Day 7, Grade C) gösteren embriyoların, uygun klinik stratejilerle sağlıklı doğumlara imkân tanıyabildiği kanıtlanmıştır; nitekim modern tıpta “kullanılamaz/atık” yaklaşımının yerini, “düşük potansiyelli ancak kullanılabilir” embriyo tanımına bıraktığı gözlemlenmektedir. Her embriyonun, hasta yaşı ve klinik öykü gibi bireysel faktörlerle birlikte bütüncül bir yaklaşımla değerlendirilmesi esastır. Laboratuvar süreçlerinde ise, her bir embriyonun gelişimsel potansiyelinin en üst düzeye çıkarılmasının hedeflendiği ve tüm işlemlerin bu hassasiyetle yürütüldüğü vurgulanmak isterim.
Kaynaklar
- The Working Group on the update of the ESHRE/ALPHA Istanbul Consensus. (2025). The Istanbul consensus update: a revised ESHRE/ALPHA consensus on oocyte and embryo static and dynamic morphological assessment. Human Reproduction.
- Coticchio, G., et al. (2018). Focused time-lapse analysis reveals novel aspects of human fertilization… Human Reproduction.
- Paulson, R. J. (2011). Introduction: Assessing the embryo… Fertility and Sterility.
- Swain, J. E. (2019). Controversies in ART: considerations and risks for uninterrupted embryo culture. Reproductive BioMedicine Online.
- Bamford, T., et al. (2022). Morphological and morphokinetic associations with aneuploidy… Human Reproduction Update.
- Gardner, D. K., & Schoolcraft, W. B. (1999). In-vitro culture of human blastocysts.
- Cimadomo, D., et al. (2022). How slow is too slow? A comprehensive portrait of Day 7 blastocysts. Human Reproduction.
- Rosenbusch, B., et al. (2002). Cytogenetic analysis of giant oocytes… Human Reproduction.
- Capalbo, A., et al. (2017). Abnormally fertilized oocytes can result in healthy live births… Fertility and Sterility.
- Rhenman, A., et al. (2015). Which set of embryo variables is most predictive for live birth? Human Reproduction.
- Hardarson, T., et al. (2001). Human embryos with unevenly sized blastomeres… Human Reproduction.
- Hung, T. Y., et al. (2018). Early blastulation of day 4 embryo correlates with the increased euploid rate… Taiwanese Journal of Obstetrics and Gynecology.
- Alpha Scientists in Reproductive Medicine and ESHRE Special Interest Group Embryology. (2011). Istanbul consensus workshop on embryo assessment.
- Subira, J., et al. (2016). Grade of the inner cell mass, but not trophectoderm, predicts live birth… Human Fertility.
- Ahlström, A., et al. (2011). Trophectoderm morphology: an important parameter for predicting live birth… Human Reproduction.
- Liu, L., et al. (2023). Multimodal blastocyst evaluation using AI and clinical features. eLife.
- Du, T., et al. (2018). Fertility and neonatal outcomes of embryos achieving blastulation on Day 7… Human Reproduction.
- Kieslinger, D. C., et al. (2023). Clinical outcomes of uninterrupted embryo culture with or without time-lapse-based embryo selection… The Lancet.
- Kato, K., et al. (2023). Deep learning models for pregnancy prediction in IVF. Reproductive BioMedicine Online.
- Diakiw, S. M., et al. (2022). An artificial intelligence model correlated with morphological and genetic features… Reproductive BioMedicine Online.
- Capalbo, A., et al. (2014). Correlation between standard blastocyst morphology, euploidy and implantation… Human Reproduction.
- Viotti, M., et al. (2021). 1000 Mosaic embryo transfers: a prospective study… Fertility and Sterility.
- ASRM Practice Committee. (2023). Clinical management of mosaic results from PGT-A… Fertility and Sterility.
- Franasiak, J. M., et al. (2014). The nature of aneuploidy with increasing age… Fertility and Sterility.
- Wang, Y., et al. (2024). Effects of maternal age… on pregnancy outcomes. Frontiers in Endocrinology.
